Atelier 1 : Construction, observation et fonctionnement d'une pile au citron
PDF - 2 323 ko
Se sensibiliser aux composants chimiques et métalliques de la pile.
Repérer sur un schéma de pile les différents éléments mis en scène dans l’expérience.
Pour construire et voir fonctionner une pile au citron, il vous faut :
Vous trouverez les vis galvanisées, le fil électrique ainsi que les diodes dans n’importe quel magasin de bricolage.
La carte postale musicale se trouve dans les boutiques cadeau et carterie.
Veillez, avant l’installation, à ce que les pièces de monnaie et les vis soient bien brillantes.
Si ce n’est pas le cas, frottez-les avec un peu de paille de fer.
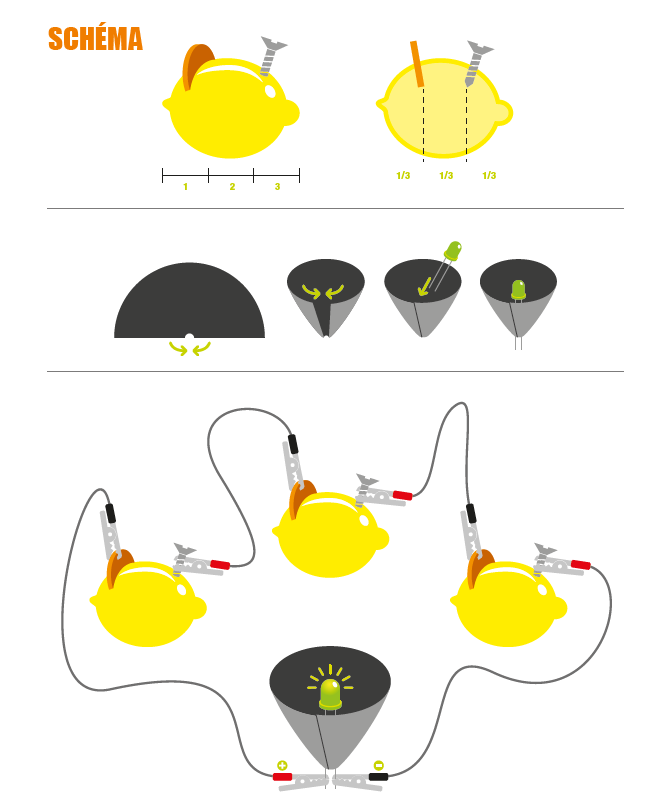
Option : L’effet de la pile au citron peut aussi être mis en évidence avec une carte postale musicale d’anniversaire.
Découpez le papier qui enserre le dispositif, retirez la pile existante et fixez l’extrémité des fils électriques sur les bornes positives et négatives
(prenez soin de retirer les pinces crocodiles pour cette opération).
Une pile fonctionne grâce à une réaction chimique entre deux matières. L’une peut céder facilement des électrons (ici, c’est la vis zinguée), et l’autre peut les attirer (ici c’est la pièce en cuivre).
Chaque matériau est une électrode. Ces électrodes, lorsqu’elles sont reliées à un consommateur électrique (ici, la diode), provoquent la circulation d’électrons, c’est le courant électrique ; c’est la réaction chimique provoquée par l’acide du citron qui induit une circulation de charges positives et négatives (électrons, ions). Une pile fournit donc du courant continu.
La borne négative d’une pile correspond à l’anode, c’est elle qui fournit les électrons.
La borne positive d’une pile correspond à la cathode, c’est elle qui consomme les électrons.
Etapes
Lorsque la vis zinguée entre en contact avec l’acide citrique du citron, il se passe deux choses : l’acide attaque les atomes de zinc et les transforme en ions zinc (Zn2+), chargés positivement (ce sont eux qui noircissent la surface autour de la vis). Cela libère aussi deux électrons (2e-), chargés négativement.
Par ailleurs, la réaction chimique produit des ions hydrogène chargés positivement et formant un gaz : on voit des petites bulles autour de la vis. Ces ions aident à détacher les électrons négatifs du zinc (ils s’attirent comme des aimants !).
Au contact de l’acide du citron, le cuivre des pièces se charge positivement (Cu2+). Ces charges positives, légèrement plus puissantes que celles des ions hydrogène présents dans l’acide citrique, attirent la plupart des électrons détachés du zinc.
Toutefois, pour que les électrons circulent, il faut une connexion entre la pièce en cuivre et la vis zinguée. Dès qu’un chemin conducteur (ou un circuit) est établi entre cette vis et le centime en cuivre, le cuivre attire les électrons hors de la vis via le circuit, puis les renvoie dans le citron via la pièce. C’est le courant électrique qui peut allumer la diode !
La tension de la pile électrique au citron provient de la différence relative qui existe entre la faculté du zinc et celle du cuivre à perdre leurs électrons. Le courant électrique fourni par la pile dépend notamment
de la quantité d’électrons libérés suite aux réactions chimiques.